Реализация системных мероприятий МКП в трех областях хирургической медицины потенциально позволит ежегодно экономить множество литров крови в пользу не имеющих альтернативы клинических ситуаций.


Дефицит железа/железодефицитная анемия (ДЖ/ЖДА) оказывают значимое потенциальное влияние на масштабы краткосрочных/долгосрочных потерь здоровья и преждевременной смертности, обеспечивая тем самым большой вклад в суммарный связанный с нездоровьем социально-экономический ущерб общества1.
По оценке Всемирной организации здравоохранения, последствия железодефицитной анемии для здоровья часто скрыты, но при этом незаметно снижают потенциал развития отдельных людей, обществ и национальных экономик2.



В России доля от связанных с ДЖ/ЖДА потерь (YLD ЖДА) составляет в среднем ~1,03% (211,5 тыс. лет жизни) от общих годовых не фатальных потерь РФ от всех заболеваний/состояний (20,53 млн лет жизни) с долей женщин 59,95%, мужчин — 40,1% 5.
Бóльшая часть потерь в связи с ЖДА (85,7%) приходится на основной трудоспособный возраст (15–49 лет).
РАСПРОСТРАНЕННОСТЬ ДЖ/ЖДА ПО ПОЛУ И ВОЗРАСТУ, РФ, 20176


Особое значение вовлеченность работоспособного российского населения в проблему ДЖ/ЖДА приобретает в контексте общих потерь этой возрастной группы от различных заболеваний/состояний, резко контрастирующих с общими потерями в большинстве развитых стран мира.

Если показатели общественного здоровья (заболеваемость, распространенность, смертность) оцениваются по данным обращаемости за медицинской помощью в случае болезни, то многие патологические состояния, к которым относятся и дефицит железа/железодефицитная анемия, диагностируются случайно или развиваются как сопутствующие при иных заболеваниях.



Многофакторная природа патогенеза дефицита железа и анемии при ряде заболеваний затрудняет дезагрегированную оценку его бремени, в том числе у хирургических пациентов. В недавнем исследовании Института экономики здравоохранения НИУ ВШЭ эта трудность была преодолена посредством построения эконометрических моделей и использования данных GBD, что позволило с высокой степенью достоверности выявить взаимосвязь независимых переменных и на этой основе рассчитать скрытое социально-экономическое бремя последствий нескорректированного ДЖ/ЖДА у пациентов в трех хирургических областях медицины: колопроктологии (С18, С19–21, МКБ-10), сердечно-сосудистой хирургии (I20–I25) и акушерстве7,8,9.
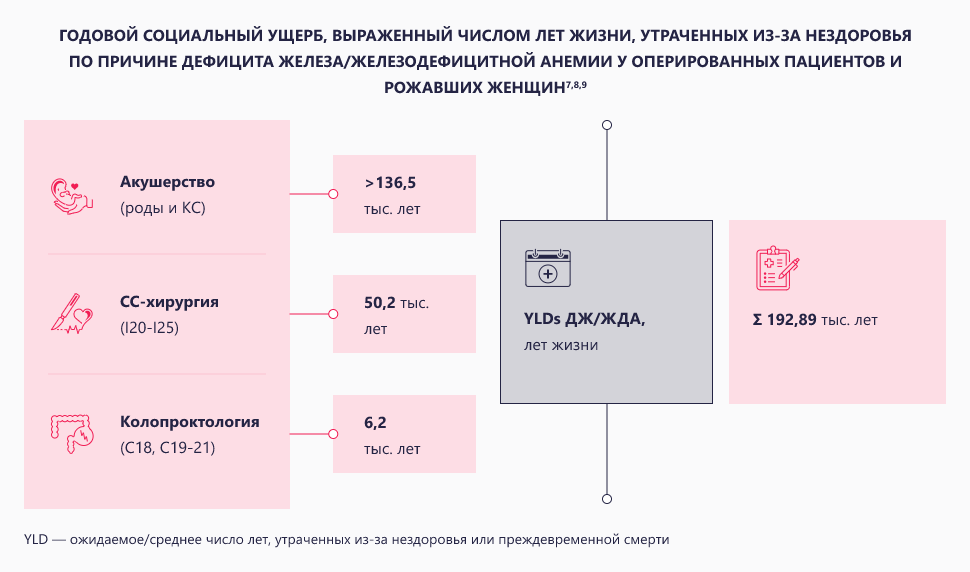
Потенциальный суммарный ущерб в связи с периоперационными ДЖ/ЖДА, рассчитанный для годового объема выполняемых в РФ плановых и экстренных операций при определенных заболеваниях в трех хирургических областях медицины, составляет 192,89 тыс. потенциально потерянных лет жизни и более 93,8 млрд руб. в монетарном выражении. Средневзвешенный удельный монетарный эквивалент потерь (на каждую тысячу операций/родов с дефицитом железа/анемией) достигает 122,9 млн руб.


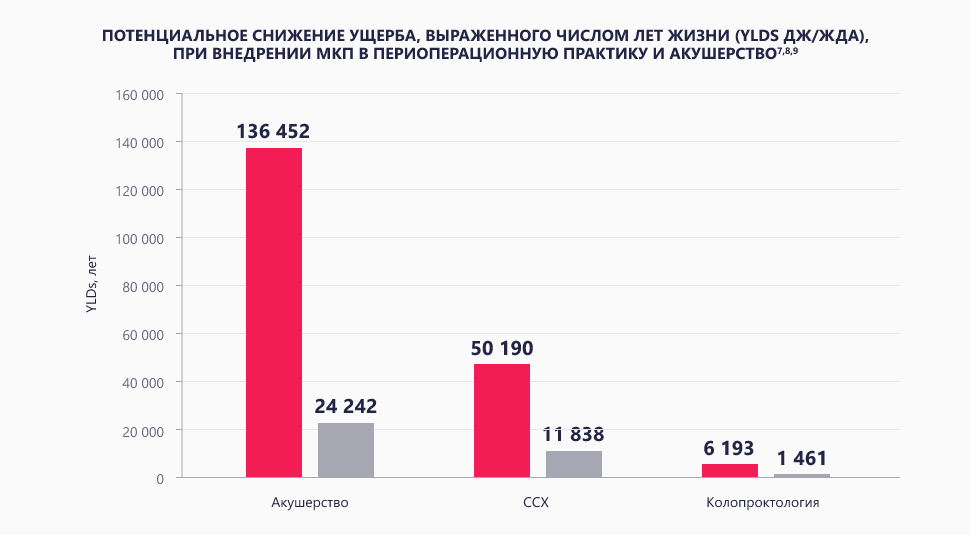


Потенциальный суммарный ущерб в связи с периоперационными ДЖ/ЖДА, рассчитанный для годового объема выполняемых в РФ плановых и экстренных операций при определенных заболеваниях в трех хирургических областях медицины, составляет 192,89 тыс. потенциально потерянных лет жизни и более 93,8 млрд руб. в монетарном выражении. Средневзвешенный удельный монетарный эквивалент потерь (на каждую тысячу операций/родов с дефицитом железа/анемией) достигает 122,9 млн руб.





Оценка влияния мероприятий менеджмента крови пациентов на некоторые финансовые показатели здравоохранения представляет практический интерес для организаторов здравоохранения, руководителей службы крови, страховых компаний.
В научной периодике представлены результаты многих исследований, показывающих не только масштабы расходов здравоохранения на преодоление последствий своевременно нескорректированного ДЖ/ЖДА у хирургических пациентов, но и выгоды здравоохранения от внедрения системы МКП.
- Швейцарские исследователи продемонстрировали, что комплексный менеджмент крови пациентов способен существенно снизить не только частоту трансфузий препаратов крови, но и связанные с ними потери и затраты. За четыре года реализации программы МКП в одной из швейцарских клиник количество переливаний аллогенных препаратов крови уменьшилось на 35% с наиболее устойчивым эффектом (на 40%) для эритроцитов, что позволило ежегодно экономить CHF 3,2 млн ($3,1 млн) на их приобретение.

- Еще более впечатляющие по срокам достижения после внедрения программы МКП результаты были продемонстрированы в университетской клинике Цюриха, где в течение первого года переливание всех аллогенных препаратов крови из расчета на 1000 пациентов снизилось на 27%, а количество доз — с 9 до 7 (р <0,001), с экономией более $2,0 млн.

Вклад МКП (включая в/в введение препаратов железа) на показатели переливания препаратов крови и связанных с этим затрат:
- Одна из самых успешных программ МКП реализована австралийской национальной системой здравоохранения. Ее результаты представлены в крупнейшем ретроспективном исследовании (605 046 пациентов в четырех крупных больницах Западной Австралии, 2008–2014 гг.), подтвердившем связь МКП с улучшением результатов лечения пациентов, снижением использования препаратов крови и связанных с ними затрат.
За шесть лет реализации программы число плановых оперативных вмешательств у пациентов с нескорректированной анемией снизилось на 20,8% (с 35,2% до 14,4%, р = 0,001), общий объем трансфузий — на 41% (р < 0,001), в т. ч. эритроцитарной массы — на 41%, СЗП — на 47%, тромбоцитарной массы — на 27%. Снижение частоты и объемов трансфузий препаратов крови обеспечило экономию в размере AU $18,5 млн ($18,8 млн). Кроме того, за счет сокращения пребывания пациентов в стационаре (коэффициент заболеваемости 0,85; 0,84–0,87; p < 0,001), снижения внутрибольничных инфекций (OR 0,79; 0,73–0,86; p < 0,001), госпитальных сосудистых осложнений — ОИМ, инсульт (OR, 0,69; 0,58–0,82; p < 0,001) и госпитальной смертности (OR 0,72; 0,67–0,77; p < 0,001) расходы системы здравоохранения Западной Австралии снизились на AU$ 80–100 млн ($78–97млн).

- В 2019 году для оценки результирующего воздействия МКП был проведен масштабный метаанализ, включивший семнадцать исследований (235 779 хирургических пациентов). Внедрение мультимодальных мер МКП привело к средней экономии 0,43 единиц эритроцитов на пациента (MD -0,43; -0,54 до -0,31, P <0,00001), частота переливаний снизилась на 39% (ОР 0,61, 0,55–0,68, P <0,00001). В среднем, на 0,45 дня уменьшилась средняя продолжительность пребывания пациентов в стационаре (MD -0,45; -0,65 до -0,25, P <0,00001), на 20% — общее число осложнений (ОР 0,80; 0,74–0,88,P <0,00001), на 11 % — смертность (ОР 0,89; 0,80–0,98, P = 0,02).
- В рамках еще одного метаанализа, опубликованного в 2020 году, был проведен анализ затрат и выгод здравоохранения при МКП (более 235 000 пациентов). По результатам снижения трансфузий эритроцитов (с 29,9% до 18,24%), среднего числа перелитых единиц на пациента (с 1,67 до 1, 25) и средней длительности пребывания в стационаре (с 9,98 до 9,53 дней) средняя стоимость переливания эритроцитов на одного пациента была снижена более чем на 50%, а снижение частоты трансфузий и длительности пребывания пациентов в стационаре позволили сэкономить €150,64 на пациента. Общий возврат инвестиций в МКП (общая выгода) составил €21,60 на каждого хирургического пациента или €1,9 млн на 100 тыс. моделируемых пациентов.

Расчеты по российским данным в настоящее время проводятся исключительно в рамках имитационных моделей в силу отсутствия реальных показателей МКП как системы, до настоящего времени не реализованной в РФ (система не получила пока достаточного распространения в РФ). Тем не менее, проведенные модельные расчеты показывают, что индивидуальное управление кровью пациентов в трех областях хирургической медицины потенциально выгодно для прикладной экономики здравоохранения.




При выборе препаратов для восполнения дефицита железа/железодефицитной анемии у хирургических пациентов исходят из необходимости получения быстрого эффекта: восстановление запаса железа и концентрации гемоглобина до целевых показателей позволяет выполнить хирургическое вмешательство в запланированные сроки. Поэтому в настоящее время наиболее эффективным терапевтическим подходом считается внутривенное введение препаратов железа.


В российском здравоохранении наиболее распространены железосахарозные комплексы (ЖСК) и карбоксимальтозат железа (КМЖ), демонстрирующие высокую клиническую результативность, но имеющие ряд различий:
- по составу углеводной оболочки
- по молекулярной массе
- по скорости высвобождения железа
- по постинъекционному клиренсу
- по максимально переносимой разовой дозе
- по допустимой скорости введения
- по иммуногенности
- по стоимости





Введение больших доз железа при меньшем количестве инфузий экономически выгодно для всех подразделений медицинских учреждений. Снижение расходов в стандартных условиях дневного стационара (в 1,4 раза) а также терапевтического и хирургического отделений круглосуточного стационара (в 3,0 и 3,8 раз соответственно) компенсирует более высокую закупочную стоимость препарата КМЖ по сравнению с любым из трех железосахарозных комплексов.
Коэффициенты затратной эффективности (CER) для препарата КМЖ на один случай коррекции анемии с полным или частичным восполнением дефицита железа без побочных эффектов в разных организационных условиях ниже минимальных значений CER для препарата ЖСК (Сотекс) из всех препаратов ЖСК: на 44,1% в дневном стационаре, на 297,1% в терапевтическом отделении, на 219,5% в хирургическом отделении. В сравнении с двумя другими препаратами ЖСК (Вифор Фарма) и ЖСК (Велфарм) затратная эффективность КМЖ еще ниже.


С этих же позиций его следует считать препаратом выбора при вынужденном предоперационном пребывании пациентов в круглосуточном стационаре и при необходимости послеоперационной коррекции дефицита железа/анемии.
- Потери в связи с уменьшением продолжительности жизни, сокращением трудоспособного периода связи с заболеваемостью, инвалидизацией или смертностью.
- WHO/UNICEF/UNU. Iron deficiency anemia: assessment, prevention and control, a guide for programmе managers. WHO, 2001.
- Murray Christopher J.L., Phil D., Lopez Alan D. Measuring the Global Burden of Disease. N Engl J Med 2013; 369: 448–57. Global Burden of Disease (GBD) — совместный проект ВОЗ и Всемирного банка.
- Kassebaum N.J. on behalf of GBD 2013 Anemia Collaborators. The Global Burden of Anemia. Hematology/Oncology Clinics of North America. 2016, V.30, Is.2, 247–308.
- GBD 2017. IHME, 2018 http://ghdx.healthdata.org/gbd-results-tool.
- Ширяева Я.Д. Ненаблюдаемая экономика и ее оценка. Экономический вестник Ростовского государственного университета.2009, т.7. — №2. — 82–97.
- Голухова Е.З., Купряшов А.А., Хичева Г.А., Куксина Е.В., Волкова О.И., Курилович Е.О., Попович Л.Д. Оценка социально-экономических выгод от внедрения менеджмента крови пациентов в практику оперативных вмешательств по поводу ишемической болезни сердца (I20–I25). Кардиология. 2021; 61(3): 77–86.
- Курилович Е.О., Волкова О.И., Федорова Т.А., Голубцов В.В., Попович Л.Д., Андреева М.Д., Барковская Н.А., Шмаков Р.Г., Ахиджак А.Н., Хамидулина К.Г. Социально-экономические выгоды адекватной коррекции дефицита железа у беременных. Акушерство и Гинекология.
- Веселов А.В., Кашников В.Н., Курилович Е.О., Шкурко Т.В., Туктагулов Н.В., Волкова О.И., Попович Л.Д. Модельная оценка социально-экономического эффекта от внедрения мероприятий менеджмента крови пациентов для коррекции предоперационного дефицита железа / железодефицитной анемии при колоректальном раке. Доказательная гастроэнтерология.
- Израсходованные обществом ресурсы в связи с заболеваемостью, инвалидизацией или смертностью.
- Прохоров Б.Б., Шмаков Д.И. Оценка стоимости статистической жизни и экономического ущерба от потерь здоровья//Проблемы прогнозирования. — 2002. № 3. — С. 125–135.
- Ревич Б.А., Авалиани С.Л., Бобылев С.Н., Сафонов Г.В., Сидоренко В. Методические указания. Экономическая оценка потерь здоровья населения в результате воздействия неблагоприятных факторов окружающей среды. 2006.
- Hofmann A, Farmer S, Towler SC. Strategies to preempt and reduce the use of blood products: an Australian perspective. Curr Opin Anaesthesiol. 2012 Feb; 25(1): 66–73.
- Kaserer A., Rössler J., Braun J., Farokhzad F., Pape H.‐C., Dutkowski P., Plass A., Horisberger T., Volbracht J., Manz M.G., Spahn D.R. Impact of a Patient Blood Management monitoring and feedback programme on allogeneic blood transfusions and related costs. Anaesthesia. 2019, Vol.74, Iss.12, 15340–1541.
- Mehra T, Seifert B, Bravo-Reiter S, Wanner G, Dutkowski P, Holubec T, Moos RM, Volbracht J, Manz MG, Spahn DR. Implementation of a patient blood management monitoring and feedback program significantly reduces transfusions and costs. Transfusion. 2015 Dec;55(12):2807-15.
- Leahy MF, Hofmann A et al. Improved outcomes and reduced costs associated with a health‐system–wide patient blood management program: a retrospective observational study in four major adult tertiary‐care hospitals. 2017, Vol 57, Iss 6, 1347–1358.
- Althoff FC, Neb H, Herrmann E, et al.: Multimodal patient blood management program based on a three-pillar strategy: a systematic review and metaanalysis. Ann Surg 2019; 269: 794–804.
- Meybohm P, Straub N, Fullenbach Ch, Judd L, Kleineruschkamp A, Taeuber Il, Zacharowski K, Choorapoikayil S. Health economics of Patient Blood Management: a cost-benefit analysis based on a meta-analysis. Vox Sanguinis,2020, 115, 182–188.
- Muñoz M, Gomez-Ramirez S, Garcia-Erce JA.) Intravenous iron in inflammatory bowel disease. World Journal of Gastroenterology: WJG 2009; 15(37): 4666–74.
- Инструкция по применению препарата Феринжект®, https://www.vidal.ru/drugs/ferinject__29503.
- Моисеев С.В. Железа карбоксимальтозат (Феринжект®) – новый внутривенный препарат для лечения железодефицитной анемии. Клин фармакол тер 2012; 21(2): 48–53.
- Khalafallah AA, Yan C, Al-Badri R, Robinson E, Kirkby BE, Ingram E, Gray Z, Khelgi V, Robertson IK, Kirkby BP. Intravenous ferric carboxymaltose versus standard care in the management of postoperative anemia: a prospective, open-label, randomised controlled trial. Lancet Haematol. 2016 Sep; 3(9): 415–25.
- Курилович Е. О., Волкова О. И., Попович Л. Д. Клинико-экономические аспекты применения парентеральных препаратов железа для коррекции дефицита железа и анемии у пациентов хирургического профиля. ГлавВрач. 2020; 7: 44–54.
